更新时间:2016-04-22 17:02 浏览: 次 作者:admin 文章来源:未知

CRISPR/Cas9基因编辑技术这两年可谓红遍大江南北。2015年,仅国家自然基金中以此技术为主要关键词申请成功的项目,金额总和就高达2282万。CRISPR“一哥”张峰博士近期再度发力,其团队9月25日《CELL》发文,即发现CRISPR另一个非常强大的效应分子——Cpf1。此类全新的基因编辑系统,CRISPR/Cpf1,有望开启新一代基因编辑技术热潮。
1.传统的CRISPR/Cas9是怎么工作的。
2.CRISPR/Cpf1和CRISPR/Cas9相比有什么不同,存在什么优势。
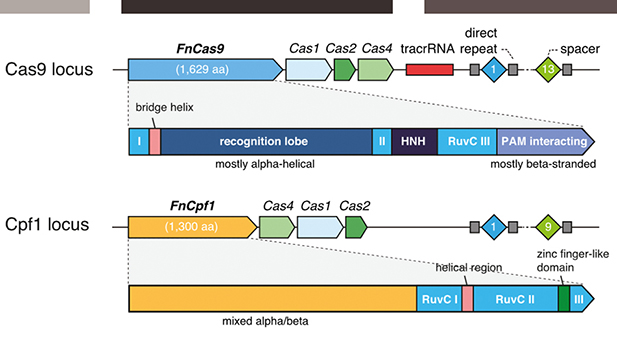
同CRISPR/Cas9系统中Cas9一样,新发现的Cpf1同属于2型效应器。但两者在结构上还是存在较大差异的。Cpf1缺少HNH核酸内切酶结构域,仅含有RuvC。同时Cpf1中Cas1,Cas2和Cas4编码氨基酸序列,和1、3型CRISPR系统更相近。
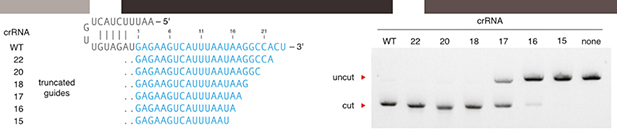
Cpf1发挥核酸内切酶作用,仅仅需要crRNA引导,不需要tracrRNA;这应该是Cpf1和Cas9最显著的区别;同时,Cpf1识别的crRNA序列长度(~42nt)比传统Cas9系统识别的crRNA序列长度更短。
优势:Cpf1体积更小,更容易进入细胞。仅需要设计crRNA,简化了设计过程。crRNA长度短,更利于合成,节约成本。同时,Cpf1需要的crRNA引导序列短,能够加强基因编辑的深度和准确度。
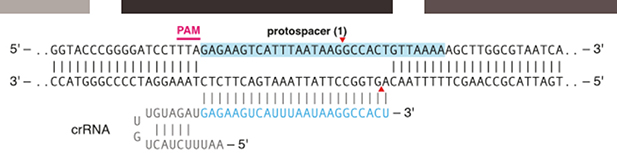
Cpf1切割目标序列能够切割出5’突出的黏端切口,Cas9只能切出平端;
优势:切割产生的5'hang out利于外源基因的插入,更容易保证插入序列的方向性;在非分裂细胞中,HDR作用机制(多发生在真核细胞G2和S期)很难发挥作用。Cpf1可以利用非HDR机制很好的解决这个问题。
Cpf1的切割位点距离种子区域很远。
优势:切割位点远离种子区域,更利于基因编辑中保留种子区域,方便针对同一靶序列的二次切割,这点Cas9无法做到。
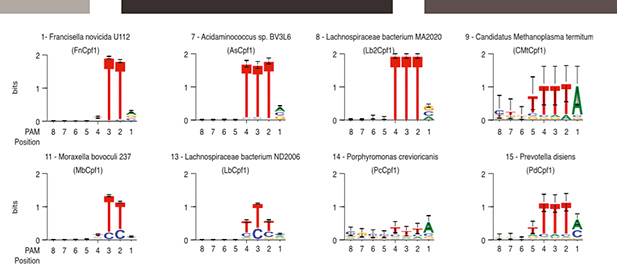
Cpf1识别T-rich PAM序列,目前所有的哺乳动物基因编辑蛋白识别位点中至少含有1个G核苷酸。Cpf1的发现无疑扩充了此类基因编辑系统的使用价值。